Internacional
- Publicada em 13 de Abril de 2021 às 17:01EUA pede pausa em vacina da Johnson & Johnson após relato de coágulos
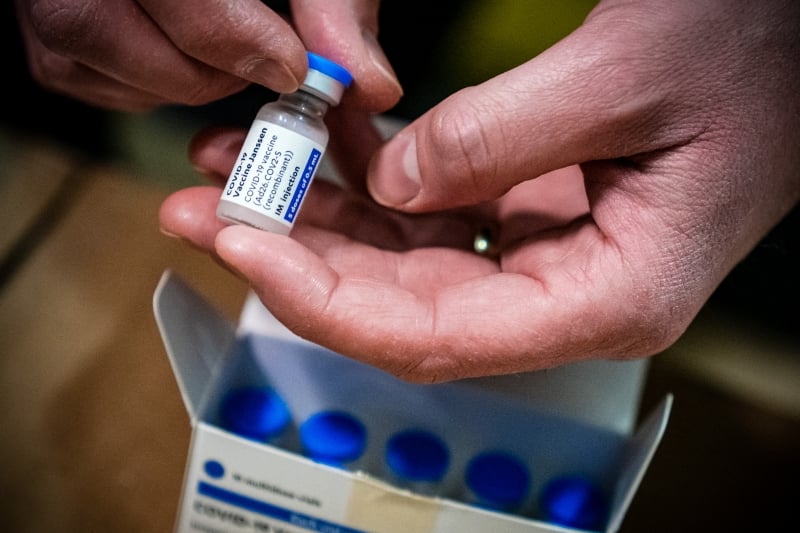
Vacina da Johnson &Johnson é de dose única, enquanto a maioria é aplicada em duas doses
ROB ENGELAAR/ANP/AFP/JC
Agências federais de saúde dos Estados Unidos (EUA) recomendaram nesta terça-feira (13) uma pausa na aplicação da vacina contra a Covid-19 da Johnson & Johnson, depois de seis pessoas que a receberam desenvolverem um distúrbio raro envolvendo coágulos sanguíneos.
Quer continuar lendo este e outros conteúdos sérios e de credibilidade?
Assine o JC Digital com desconto!
Assine o JC Digital com desconto!
- Personalize sua capa com os assuntos de seu interesse
- Acesso ilimitado aos conteúdos do site
- Acesso ao Aplicativo e versão para folhear on-line
- Conteúdos exclusivos e especializados em economia e negócios
- Cancelamento on-line e a qualquer momento
Agências federais de saúde dos Estados Unidos (EUA) recomendaram nesta terça-feira (13) uma pausa na aplicação da vacina contra a Covid-19 da Johnson & Johnson, depois de seis pessoas que a receberam desenvolverem um distúrbio raro envolvendo coágulos sanguíneos.
A medida é adotada menos de uma semana depois de reguladores europeus afirmarem que encontraram uma possível relação entre a vacina contra a Covid-19 da AstraZeneca e um problema raro de coágulos sanguíneos, que levou a um pequeno número de mortes.
A vacina de dose única da Johnson & Johnson - a maioria das vacinas contra a Covid-19 é aplicada em duas doses - e o imunizante de baixo custo da AstraZeneca são vistos como ferramentas vitais contra uma pandemia que já causou mais de 3 milhões de mortes.
O Centro de Controle de Doenças dos Estados Unidos (CDC) fará uma reunião na quarta-feira (14) para analisar os casos relacionados à vacina da J& J e a agência reguladora Foods and Drugs Administration (FDA) revisará a análise, disseram os dois órgãos em comunicado conjunto.
As seis pessoas que receberam a vacina e desenvolveram o distúrbio raro são mulheres na faixa de 18 a 48 anos, e os sintomas surgiram entre seis e 13 dias após a aplicação. Nos casos, um tipo de coágulo sanguíneo chamado trombose de seios venosos cerebrais foi detectado, em combinação com baixo nível de plaquetas sanguíneas.
O CDC e a FDA disseram que os eventos adversos parecem ser extremamente raros. A J& J disse estar trabalhando próxima dos reguladores e afirmou que nenhuma relação causal clara foi estabelecida entre os eventos e a vacina, feita por sua unidade farmacêutica Janssen.
Uma mulher morreu e uma segunda no estado do Nebraska, foi hospitalizada em estado grave, disse o jornal The New York Times citando autoridades. Até o dia 12 de abril, mais de 6,8 milhões de doses da vacina da J&J já haviam sido aplicadas nos Estados Unidos.
No Brasil, Anvisa aprovou autorização temporária
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou a autorização temporária para uso em caráter emergencial no Brasil da vacina da Janssen, um braço da Johnson & Johnson. O governo federal já adquiriu 38 milhões de doses do imunizante.
Seguindo a recomendação da área técnica da Anvisa, a maioria dos diretores votou pela permissão de uso, com base em uma avaliação de que os benefícios da vacina superam os riscos trazidos por ela.
Conforme a área técnica, o imunizante pode ser aplicado em pessoas com mais de 18 anos, com ou sem comorbidades. A eficácia geral demonstrada pela farmacêutica no processo de submissão foi de 66,9%. Quando considerados casos graves, a eficácia comprovada foi de 76,7% após 14 dias e 85,4% depois de 28 dias.