Coronavirus
- Publicada em 29 de Janeiro de 2021 às 15:00Vacina da Janssen de dose única é eficaz contra a Covid, mas proteção contra novas variantes preocupa
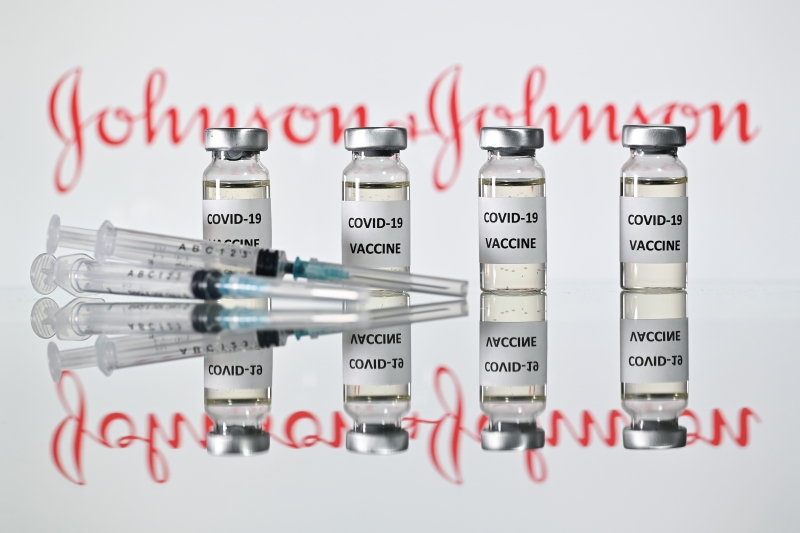
Além da dose única, a vantagem do imunizante é o armazenamento em refrigeradores comuns
JUSTIN TALLIS / AFP/ JC
A Janssen, braço do laboratório Johnson & Johnson (J&J), anunciou nesta sexta-feira (29) que sua vacina contra a Covid-19 é eficaz contra o desenvolvimento da doença com uma única dose.
Quer continuar lendo este e outros conteúdos sérios e de credibilidade?
Assine o JC Digital com desconto!
Assine o JC Digital com desconto!
- Personalize sua capa com os assuntos de seu interesse
- Acesso ilimitado aos conteúdos do site
- Acesso ao Aplicativo e versão para folhear on-line
- Conteúdos exclusivos e especializados em economia e negócios
- Cancelamento on-line e a qualquer momento
A Janssen, braço do laboratório Johnson & Johnson (J&J), anunciou nesta sexta-feira (29) que sua vacina contra a Covid-19 é eficaz contra o desenvolvimento da doença com uma única dose.
Os dados de segurança e imunogenicidade da vacina já haviam sido publicados no dia 13 de janeiro na revista científica New England Journal of Medicine, em artigo que constatou a produção de anticorpos em 98% dos participantes após uma dose única. A vacina apresentou eficácia de 85% na redução de casos graves da doença, incluindo proteção contra internações e mortes.
Os resultados divulgados nesta sexta-feira se referem aos ensaios clínicos de fase 3 do imunizante, conduzidos simultaneamente em diversos países, e são para casos moderados e graves, que necessitam de hospitalização. Ainda não há dados para proteção de casos assintomáticos ou impedir infecção do vírus.
Os números variaram também segundo a região do estudo, indicando uma possível influência das novas variantes do coronavírus no número de casos e consequente proteção da vacina.
Nos Estados Unidos, onde foram avaliados cerca de 45 mil participantes, a eficácia da vacina em impedir hospitalização foi de 72%. Na América Latina, essa taxa caiu para 66%, enquanto na África do Sul, foi menor ainda, de 57%.
O país sul-africano vem enfrentando um aumento do número de casos e mortes devido à circulação de uma nova variante, a B.1.135, caracterizada por uma série de mutações, incluindo a E484K, possivelmente associada a uma evasão do sistema imune. A linhagem, identificada primeiro nesse país, já foi detectada nos Estados Unidos.
Não foram divulgados dados do estudo da vacina para o Reino Unido, onde uma nova variante também tem causado aumento substancial no número de casos não só na região, mas também em outros países da Europa.
No Brasil, a nova variante de Manaus causa preocupação semelhante por conter as duas mutações identificadas nas variantes do Reino Unido e da África do Sul, na proteína S do Spike (ou espícula, o gancho utilizado pelo coronavírus para entrar nas células).
Se for confirmado que a baixa eficácia da vacina está associada à evasão do sistema imune pela variante da África do Sul, outras vacinas em fase final de testes ou já aprovadas para uso, como as da Pfizer/BioNTech, Moderna, Oxford/AstraZeneca e Novavax podem também apresentar o mesmo risco.
A J&J disse ainda que pretende enviar o pedido de aprovação para uso emergencial à FDA (agência norte-americana que regulamenta medicamentos) até a próxima semana, o que colocaria a vacina disponível para uso até o final de fevereiro.
O diretor científico da companhia, Paul Stoffels, disse ao New York Times que a vacina (da Janssen) é "a que pode fazer diferença no combate à pandemia com uma única dose". As demais vacinas utilizadas até o momento necessitam de duas doses, em um intervalo de 21 dias, para garantir os índices de proteção.
O anúncio vem em um momento em que a administração do novo presidente americano Joe Biden tenta acelerar a taxa de vacinação nos Estados Unidos, ainda com uma escassez de doses para imunizar toda a população. Autoridades da Casa Branca estão confiantes que a vacina da J&J será o caminho para minimizar essa escassez, mas a farmacêutica pode ter apenas 7 milhões de doses prontas para uso até a decisão da FDA de aprovação, segundo oficiais de saúde familiarizados com a produção da empresa, e cerca de 30 milhões até abril.
Com o avanço das novas variantes e crescente preocupação das autoridades de saúde que a situação descontrolada da pandemia possa afetar as campanhas de vacinação, especialistas têm enfatizado a importância de vacinar o maior número de pessoas em um curto período de tempo. Diminuir a taxa de infecção do vírus pode também dirimir as variantes mais contagiosas enquanto elas ainda não são predominantes na população, prevenindo também o surgimento de novas mutações que possam trazer novos riscos à saúde.
"Se havia uma razão para vacinar o maior número de pessoas o mais rápido possível com a vacina que temos agora, esse momento é agora" disse Anthony Fauci, diretor do Instituto Nacional de Alergias e Doenças Infecciosas (Niaid) dos EUA e principal infectologista do governo. "Quanto menos pessoas se infectarem, menor a chance que damos a esse mutante [variante] em específico de se tornar dominante."
Além do controle da pandemia para conter os casos com as novas variantes, os EUA têm discutido a fabricação e aceleração na produção de doses de vacinas no menor tempo possível.
Os agentes regulatórios no país aguardam dados da companhia sobre a fábrica construída em Baltimore, Maryland, que pode produzir o imunizante em larga-escala, com a possibilidade de entregar 100 milhões de doses até junho.
Se a J&J conseguir entregar as vacinas rapidamente para o governo norte-americano, a incidência de novos casos pode diminuir e, consequentemente, as chances de novas variantes se estabelecerem e piorarem a situação já fragilizada da pandemia. Como a vacina necessita de apenas uma dose para garantir a proteção, essa capacidade de produção garantiria a vacinação de 100 milhões de indivíduos.
Além da dose única, outra vantagem do imunizante seria o seu armazenamento em refrigeradores comuns, em temperaturas de 2°C a 8°C, em comparação às vacinas da Pfizer e da Moderna, que precisam ser armazenadas em ultracongeladores, a -70°C e -20°C, respectivamente.
No Brasil, a vacina da Janssen é testada em cerca de 7.000 voluntários. Em janeiro, a Anvisa concedeu o certificado de boas práticas de fabricação à companhia. A conclusão e divulgação dos ensaios clínicos no país ainda são aguardadas.
Folhapress