Coronavirus
- Publicada em 10 de Janeiro de 2021 às 09:13Aprovação da Coronavac não está sob risco, afirmam ex-presidentes da Anvisa
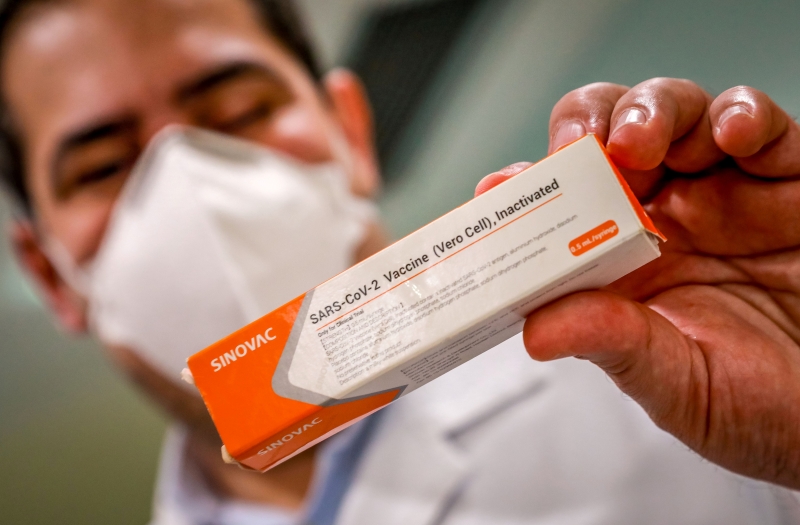
Para os especialistas, a única informação solicitada que pode apresentar algum tipo de preocupação é a de imunogenicidade do estudo fase 3
SILVIO AVILA/AFP/JC
Agência Estado
Para ex-presidentes da Agência Nacional de Vigilância Sanitária (Anvisa), a relação de documentos que falta para avaliar o pedido de uso emergencial da Coronavac, a vacina contra a covid-19 desenvolvida em parceria entre o Instituto Butantan e a farmacêutica chinesa Sinovac, não coloca em risco sua aprovação emergencial.
Quer continuar lendo este e outros conteúdos sérios e de credibilidade?
Assine o JC Digital com desconto!
Assine o JC Digital com desconto!
- Personalize sua capa com os assuntos de seu interesse
- Acesso ilimitado aos conteúdos do site
- Acesso ao Aplicativo e versão para folhear on-line
- Conteúdos exclusivos e especializados em economia e negócios
- Cancelamento on-line e a qualquer momento
Para ex-presidentes da Agência Nacional de Vigilância Sanitária (Anvisa), a relação de documentos que falta para avaliar o pedido de uso emergencial da Coronavac, a vacina contra a covid-19 desenvolvida em parceria entre o Instituto Butantan e a farmacêutica chinesa Sinovac, não coloca em risco sua aprovação emergencial.
Fundador e ex-presidente da Anvisa, o sanitarista Gonzalo Vecina Neto afirma que os dados solicitados são básicos - e ele se surpreendeu por não constarem do documento inicial entregue. "Os dados são fundamentais e apenas posso acreditar que já foram oferecidos, mas com uma estrutura diferente. Devemos esperar a manifestação do Butantan", afirma.
Para Cláudio Maierovitch, que dirigiu a Anvisa entre 2003 e 2005, a agência "está agindo corretamente" ao pedir os documentos que faltam. "São coisas simples e eu acredito que o Instituto Butantan tenha essas informações. É normal faltar documentos e suponho que tudo esteja pronto."
Entre os dados solicitados estão características básicas como: idade, sexo, raça, peso ou IMC. "Sempre que se faz um estudo de medicamento qualquer característica que possa ser importante tem de ser avaliada de forma que não haja diferença no grupo vacinado e no grupo placebo", explica Maierovitch.
Essas informações devem ser apresentadas na ficha de cada participante do estudo. Geralmente, o banco de dados é construído durante a inscrição das pessoas e, caso isso não tenha acontecido, trata-se de uma grande falha. "É importante saber, por exemplo, quantas pessoas entraram em cada fase do estudo. Se existe alguma diferença entre o grupo vacinado e o grupo que recebeu placebo, quem abandonou o estudo e os motivos", diz Maierovitch. "Uma vez que se inicia o estudo, nem tudo é encaminhado como se espera. É preciso explicar o que aconteceu."
Para os especialistas, a única informação solicitada que pode apresentar algum tipo de preocupação é a de imunogenicidade do estudo fase 3. É imprescindível que o Instituto forneça informações sobre os exames de quem desenvolveu anticorpos e medir como foi gerada essa imunidade.
"Aparentemente o Butantan simplesmente disse que vai providenciar os dados. De qualquer forma, todas as informações são importantes e devem ser apresentadas e a opinião do instituto é fundamental", complementa Vecina.
Documentos solicitados pela Anvisa:
- Características demográficas e basais críticas da população do estudo (idade, sexo, raça, peso ou IMC) e outras características (por exemplo, função renal ou hepática, comorbidades). Essas características demográficas e basais críticas devem ser apresentadas por braços do estudo e tipo de população de análise "intenção-de-tratamento" (ITT) e "por protocolo"(PP), de forma a permitir a comparabilidade dos grupos de tratamento.
- Resultados do estudo por população de "intenção-de-tratamento" (ITT).
- Dados sobre a disposição dos participantes, com uma contabilidade clara de todos os participantes que entraram no estudo. O número de pacientes que foram randomizados e que entraram e completaram cada fase do estudo (ou cada semana/mês do estudo) devem ser fornecidos, bem como as razões para todas as interrupções pós-randomização, agrupados por tratamento e por motivo principal (perda de acompanhamento, evento adverso, pobre conformidade, etc.).
- Descrição dos desvios de protocolo ocorridos no estudo com a adequada classificação de impacto e de categoria.
- Listagem de participantes com desvios de protocolo, divididos por centro.
- Dados de imunogenicidade do estudo fase 3.